新薬開発を加速するAI共同操縦者(コパイロット):ホワイトスペース分析と知財戦略の革新
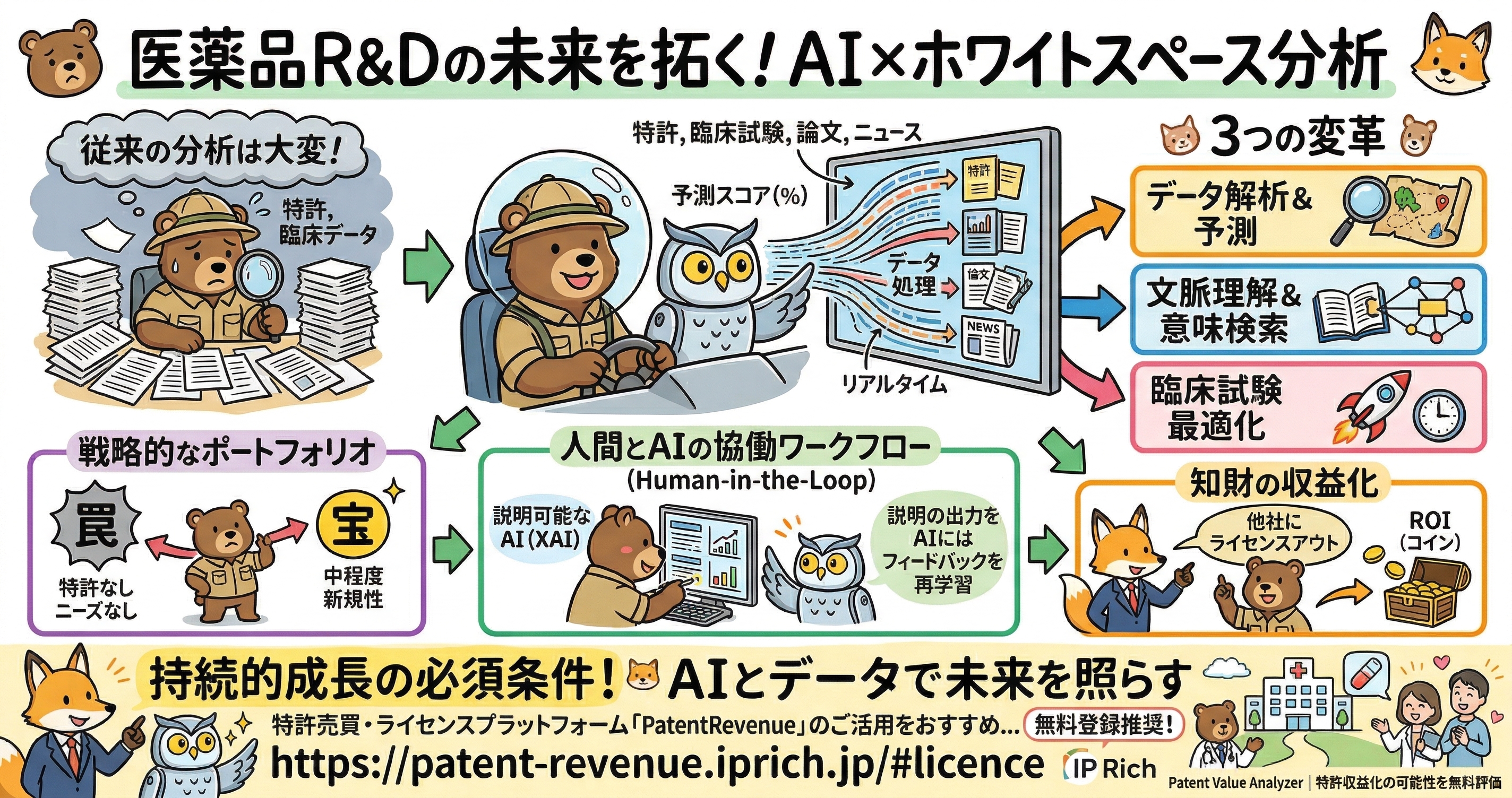
株式会社IPリッチのライセンス担当です。本日は、医薬品の研究開発(R&D)領域において近年急速にその存在感を増している「AIを共同操縦者(コパイロット)としたホワイトスペース分析」について、そのメカニズムと知財戦略への多大な影響を詳細に解説いたします。ホワイトスペース分析とは、膨大な特許出願のデータや進行中の臨床試験の動向を掛け合わせることで、技術的に未開拓でありながら市場のニーズが確かに存在する空白領域を見極めるための高度な戦略手法です。最新の人工知能(AI)技術は、自然言語処理を用いて数百万件に及ぶ特許文献や臨床データを瞬時に分類・解読し、試験の成功率や特許取得の可能性を予測する能力を備えています。本記事では、このAIが人間の分析を補完する「共同操縦者」として機能し、静的な調査報告にとどまっていたホワイトスペース分析を、未来の動向を予測する動的なインテリジェンス機能へとどのように進化させているのか、その詳細な仕組みと実践的な価値をお伝えします。
さて、こうした高度な分析を通じて見出された有望な技術領域や特許群は、単に自社での新薬開発を加速させるだけでなく、「知財の収益化」という極めて重要な経営戦略にも直結します。自社のパイプラインには合致しないものの、他社にとって価値の高い特許を発掘した場合、それらを戦略的にライセンスアウト、あるいは売却することで、多額の研究開発投資に対する迅速なリターン(ROI)を獲得することが可能です。優れた技術や特許権を保有しながらも事業化リソースに課題を抱えている場合、あるいは他社の有望な知財を導入して開発を加速させたい場合は、特許売買・ライセンスプラットフォーム「PatentRevenue」のご活用をおすすめいたします。現在、「PatentRevenue」では特許権の売買又はライセンスの希望者に無料で登録していただくことが推奨されています。ご関心のある方は、ぜひ https://patent-revenue.iprich.jp/#licence にアクセスし、知財の収益化に向けた第一歩を踏み出してください。
Patent Value Analyzer | 特許収益化の可能性を無料評価
医薬品R&Dにおけるホワイトスペース分析の変革とAIの台頭
医薬品業界は長らく、10年以上にも及ぶ長い期間と巨額の投資を要する研究開発サイクル、そしてそれに伴う極めてハイリスクな知的財産権の獲得競争によって特徴づけられてきました。このような厳しい環境下において、特定の技術分野や疾患領域における特許の空白地帯、すなわち「ホワイトスペース」を特定する取り組みは、競合他社による特許侵害のリスクを回避し、自社の独占的な市場競争力を確立するための極めて重要なプロセスとなっています。従来のホワイトスペース分析は、主に弁理士や特許調査員が手作業でデータベースを検索し、膨大な文献を読み込むことに依存しており、研究開発部門に対しては特定の時点を切り取った静的なレポートとして提出されることが一般的でした。しかし、全世界における特許文献の幾何級数的な増加と科学技術の複雑化に伴い、人間の認知能力と限られた時間のみでグローバルな知財の全体像(ランドスケープ)を網羅的に把握することは、事実上不可能となりつつあります。
ここに高度なテクノロジーが導入されることで、ホワイトスペース分析は過去の記録を追認するだけの「事後的な法的チェック」から、未来の研究開発の方向性を決定づける「予測的かつ動的なインテリジェンス機能」へと劇的なパラダイムシフトを遂げています。最新のAIプラットフォームは、世界中の特許出願、臨床試験のレジストリ、学術論文、さらには規制当局のニュースに至るまで、500以上のグローバルなデータソースを継続的かつ自動的に監視する能力を持っています。これにより、静的なレポートは過去のものとなり、競合他社による新たな特許出願、重要な臨床試験の開始や中止、あるいは競合品の臨床失敗によって突如として生まれた新たなホワイトスペースをリアルタイムで通知する動的なダッシュボードへと進化しています。
さらに、AIは特許リスクの概念そのものを再定義しています。従来の製薬企業の財務モデルにおいて、特許リスクは「特許が取得できるか、できないか」という二元的な事象として扱われてきました。しかし、機械学習モデルは特許審査の過去の履歴や引用ネットワークを学習し、対象となる化合物が非自明性(進歩性)の拒絶理由通知を克服できる確率を、連続的な確率スコアとして提示します。このスコアは、リスク調整済みの正味現在価値モデルに直接統合され、資本配分の意思決定を高度化します。研究開発の初期段階、すなわちリード化合物の選定段階においてAIを上流のフィルターとして機能させることで、すでに特許が密集している領域への無駄な投資を防ぎ、多額のサンクコスト(埋没費用)が発生する前に研究リソースを有望な白地領域へと振り向けることが可能になるのです。
特許言語の壁を越える自然言語処理(NLP)とセマンティック検索
特許文献の分析において最大の障壁となるのが、いわゆる「セマンティックギャップ(意味論的乖離)」と呼ばれる問題です。特許請求の範囲は、権利範囲を最大限に広げ、かつ競合の回避を目的として起草されるため、意図的に抽象的で難解な人工的言語体系が用いられることが多くあります。一般的な学術論文とは異なり、既知の化合物や生物学的メカニズムを表現する際にも、標準的なキーワードが意図的に避けられることすらあります。そのため、従来のキーワードの完全一致に依存したブーリアン検索などの方法では、致命的な先行技術を見落としてしまうか、あるいは膨大な無関連の特許を拾い上げてしまい、真のホワイトスペースを見極めることが極めて困難でした。
この長年の課題を根本から解決したのが、自然言語処理技術の目覚ましい進歩と、特にトランスフォーマーアーキテクチャの応用です。生命科学分野に特化してファインチューニングされた高度な言語モデルは、単語の表面的な一致ではなく、文脈や単語間の複雑な関係性を深く理解することができます。これにより、AIは特許請求の範囲に込められた技術的な意図を正確に把握し、全く異なるキーワードで記述されていても概念的に類似した先行技術を高精度で抽出するセマンティック検索を実現しました。
具体的なプロセスとしては、まず固有表現抽出技術が、膨大な非構造化テキストの中から特定の化学物質、遺伝子、タンパク質、疾患の適応症などを自動的に識別し、タグ付けを行います。次に、抽出されたこれらの要素とそれらの関係性はナレッジグラフとして構造化され、生物学的なデータと知財データの複雑な相互作用を直感的に可視化します。さらに、テキストの埋め込み手法を用いることで、特許の文や段落全体の意味的情報をベクトル空間上にマッピングし、深層学習ベースの特許ランドスケーピングを可能にしています。
また、化学構造の定量化においては、グラフニューラルネットワークが決定的な役割を果たします。グラフニューラルネットワークは化合物の分子構造をグラフとして表現し、分子間の構造的類似性や、結合親和性、毒性などの特定の物理化学的特性を予測します。特許審査、特に欧州特許庁の基準において進歩性を主張するための強力な根拠となるのが「予期せぬ技術的効果」です。特性予測モデルは、ある新規化合物が構造的に類似した先行技術から予測される以上の顕著な効果を有している可能性を事前に予測し、特許弁理士に対して進歩性の立証に向けた極めて強力な論拠を提供しています。
臨床試験データと機械学習の融合による成功予測と最適化
新薬開発における「ホワイトスペース」という概念は、単なる知財や特許の空白地帯にとどまらず、臨床試験の運用プロセスにおける「非生産的な空白時間」としても定義されます。臨床試験の要件が年々複雑化するにつれ、適格な患者の選定、プロトコルの策定、膨大なデータの収集と管理といったプロセスにおいて、手作業による逐次的な処理が開発期間の長期化を招いています。ある調査によれば、新薬開発にかかる時間のうち約45パーセントが、試験完了から次の規制当局への提出に至るまでの空白時間に費やされていると指摘されています。
こうした状況を打破するため、機械学習モデルやエージェンティックAIが臨床開発の各フェーズに本格的に導入され始めています。AIは過去の膨大な臨床試験データや電子カルテ、さらには患者レジストリなどのリアルワールドデータを横断的に学習し、最適な治験実施施設の特定や患者の登録予測をリアルタイムで行うことで、試験期間を平均して数ヶ月単位で短縮する効果をもたらしています。さらに驚くべきことに、機械学習は臨床試験の「結果そのものを予測する」能力を獲得しつつあります。
最新の報告によれば、生成AIや高度な計算プラットフォームを通じて設計されたAIネイティブな医薬品候補は、第I相の安全性試験において約90パーセントという驚異的な成功率を記録しており、業界の歴史的平均である約50パーセントを大きく凌駕しています。これに加え、疾患の進行モデルや薬効を精密にシミュレーションするツールは、サンプルサイズや試験期間などのパラメータを最適化し、規制当局からの承認を得やすい堅牢な試験プロトコルの設計を強力に支援します。
適応的治験デザインへのAIの統合も特筆すべき進化です。適応的デザインとは、試験の途中で得られた中間結果に基づいて、投与量の調整や効果のない治療群の削除、患者の再割り当てをリアルタイムで行う手法ですが、統計的な妥当性を維持するための計算が極めて複雑になります。ここに強化学習アルゴリズムやニューラルネットワークを導入することで、AIはプロトコル変更による将来の臨床的結果を瞬時に予測し、ベイズ確率の枠組みの中で第一種過誤を厳格に制御しながら意思決定を最適化します。これにより、最も有望な介入手段が迅速に特定され、臨床の場におけるホワイトスペースは極限まで削減されるのです。
人間の専門知識とAIの協働を意味する「Human-in-the-Loop」モデル
製薬業界におけるAIの導入が加速する中で、極めて重要な認識は「AIは強力な共同操縦者であり、決して完全な自動操縦装置ではない」という事実です。知財の評価や臨床的な意思決定においては、高度に文脈依存的な判断や法的なニュアンスの解釈が不可欠であり、これらをAIのアルゴリズムのみに完全に委ねることは甚大なリスクを伴います。そのため、最適なワークフローは、AIの圧倒的な処理速度およびスケーリング能力と、特許弁理士や科学者による専門的な人間の判断を融合させた「Human-in-the-Loop」モデルとして構築されるべきです。
この協働ワークフローは、機能分割された3つの明確なステージで構成されます。第1のステージでは、AIが主導して数百万件の特許文献や学術論文を数分でスキャンし、構造的類似性スコアの算出や先行技術の抽出、初期段階の特許性リスクスコアの生成を自動化します。従来、熟練の弁理士が数十時間をかけていた作業が瞬時に完了します。第2のステージでは、抽出されたAIの出力結果を人間の専門家が厳格に検証します。創薬化学者は化学構造の違いが薬理学的に意味を持つかを評価し、特許弁理士はクレーム解釈の専門知識を適用して先行技術の法的な権利範囲を精査します。そして第3のステージとして、人間による「関連あり・なし」の判断結果や修正内容がフィードバックループを通じてAIシステムに還元され、特定の技術クラスや法域の特性に合わせてモデルが継続的に再学習され、精度が向上していくのです。
この人間とAIの協働体制を真に機能させるために不可欠な技術が「説明可能なAI(XAI)」です。深層学習モデルはしばしばその推論プロセスが不透明なブラックボックスとなりますが、特許出願においては、発明がどのように機能するかを論理的に説明する実施可能要件を満たす必要があります。説明可能なAIツールは、AIが算出した特許取得確率のスコアを個別の要因に分解し、どの先行技術がリスクスコアを押し下げているか、あるいは予測されたどの分子特性がスコアを上昇させているかを弁理士に対して明確に可視化します。これにより、弁理士はAIの予測スコアを鵜呑みにするのではなく、論理的な裏付けを持って特許戦略を構築することが可能となります。
研究開発の罠の回避と中程度の新規性を狙うポートフォリオ戦略
AIとデータに基づくホワイトスペース分析は、企業が陥りがちな「研究開発の罠」を回避するための強力な羅針盤となります。戦略マトリクスにおける研究開発の罠とは、特許密度は低く技術的には未開拓であるものの、既存の治療法で十分にカバーされているため患者のアンメットメディカルニーズも低い領域を指します。この領域への投資は、技術的に特許を取得することは容易であっても、商業的な価値を生み出さない単なるサイエンスプロジェクトに終わる危険性が極めて高いのです。
このような罠に陥る最大の原因は、企業内の組織的なサイロ化にあります。知財部門が特許の空白地帯のみを追い求め、研究開発部門や商業部門が臨床的ニーズのみを別個に追求し、両者の視点が交わらない場合に致命的な投資ミスが発生します。AIプラットフォームは、特許データと臨床・市場データを統合的に解析することで、各部門の視点を強制的に同期させ、科学的に優れているが誰も必要としない解決策への資源浪費を未然に防ぐ役割を果たします。
この戦略的選定プロセスを体現しているのが、先進的なAI主導の創薬企業におけるポートフォリオ戦略です。これらの企業は、標的の新規性と技術的リスクのバランスを取るため、自社のAIプラットフォームを活用し、ターゲットを新規性の度合いに応じて分類しています。完全に未開拓で過去の臨床データが存在しない高い新規性の領域は、画期的な新薬を狙える一方で失敗リスクが極めて高くなります。そこで、明確な遺伝的検証がなされているものの、過去の薬理学的探求が限られている「中程度の新規性」の領域をスイートスポットとして集中的にターゲットする戦略が採用されています。
さらに特筆すべきは、特定されたホワイトスペースを競合他社から防衛するための知財戦略です。有望な標的が発見されると、資金力のある競合企業が類似の化合物を迅速に開発し、市場に参入してくるというファストフォロワーの脅威が常に存在します。これに対抗するため、高度な生成化学AIを活用して、発見したターゲットに対する膨大な数の有効な化学構造を網羅的に生成・列挙させ、特定の化合物の周辺に広大な「特許の網」や防衛的な公開文献を意図的に構築する取り組みが進められています。これにより、競合他社が周辺の特許を取得して参入する余地を物理的に封じ込めるという、極めて高度かつ攻撃的な知財ポートフォリオ戦略が展開されているのです。
AI発明者問題と特許要件の厳格化がもたらす知財戦略への波及効果
AIによる創薬やホワイトスペース分析の躍進は、既存の特許法制度の根幹を揺るがす深刻な法的・倫理的課題を提起しています。特許制度が直面している最も根源的かつ実存的な問いは、「AIそのものが発明者になり得るのか」という問題です。世界中で繰り広げられた法廷闘争や主要国における画期的な判決を通じて、現在の司法および特許当局は明確な見解を示しています。すなわち、特許法上の発明者は「自然人」に限られ、AIシステム単独を発明者として特許を取得することはできないという強固な法的基盤が確立されたのです。
この見解は、製薬企業の知財戦略に対して「重大な人間の貢献」という新たな要件を課すこととなりました。特許の有効性を担保するためには、単にAIの出力結果をそのまま出願するのではなく、発明の着想や具体化のプロセスにおいて、人間がいかに本質的な創造的寄与を行ったかを客観的に証明しなければなりません。具体的には、AIの探索空間を特定の解に向けて誘導するための高度に専門的なプロンプトの設計や、AIが提示した膨大な候補群の中から科学的判断に基づいて有望な化合物を選定する作業、さらにはAIの予測を検証し、予測不可能であった予期せぬ特性を発見するためのウェットラボでの実験などが、法的に評価される人間の貢献に該当します。
この人間の貢献を立証する要件は、研究開発ワークフローの設計そのものを逆転させます。従来、知財保護は研究開発の下流で行われる事後的な手続きでしたが、現在では特許を取得するための法的要件を満たすように、AIを組み込んだワークフロー自体を上流から周到に設計しなければなりません。このプロセスを支えるのが、機械学習オペレーション(MLOps)のフレームワークです。厳格な規制産業である製薬業界において、MLOpsはAIモデルの再現性を担保するだけでなく、創薬プロセスのどの段階で人間がどのような意思決定に介入したかという詳細な監査証跡を自動的に記録します。これにより、将来の特許無効審判や侵害訴訟において、人間の発明者性を客観的データとして証明する強力な防衛手段が構築されます。
また、生成AIが自律的に技術を創出する能力が高まるにつれ、企業は「特許による保護」と「営業秘密としての秘匿」の間の戦略的選択を迫られています。AIアルゴリズムそのものや、モデルの学習に用いられた独自の大規模データセットを特許出願の一環として公開することは、競合他社にコア技術を模倣されるリスクを伴います。そのため、生成された化合物自体は特許で強力に保護しつつ、その生成を導いたAIのプロンプトエンジニアリング技術や学習データセットの構造は営業秘密として隠匿するという、多層的で高度なハイブリッド知財戦略が不可欠となっています。
動的インテリジェンスが切り拓く新薬開発と知財エコシステムの未来
ここまで論じてきたように、医薬品の研究開発におけるAIを活用したホワイトスペース分析は、単なる情報の検索効率化ツールではなく、知的財産の創出、防衛、そして戦略的なポートフォリオ管理のライフサイクル全体を根底から再定義する破壊的なイノベーションです。自然言語処理技術が特許文献の難解な壁を打ち破り、機械学習が臨床試験の成功確率を定量化して可視化することで、企業は膨大な不確実性の海の中から、真に投資価値のあるホワイトスペースを高精度で特定することが可能となりました。
同時に、AIが創出する天文学的な数の化学空間は、知財ポートフォリオを単一の特許という「点」から、強固な面としての「防衛網」へと進化させ、競合他社の追随を許さない圧倒的な参入障壁を構築しています。しかし、技術が高度化する一方で、特許制度が求める人間の創造性という要件はより一層厳格さを増しています。AIを完全な自動操縦装置として盲信するのではなく、優れた共同操縦者として位置づけ、人間の専門家との緊密な協働体制を築き上げた企業のみが、激化する知財競争において真の優位性を確立することができるでしょう。
新薬開発の長期化と開発コストの高騰が続く現代において、データとAIに裏打ちされた未開拓領域への戦略的投資は、製薬企業が持続的な成長を遂げるための必須条件です。AIが動的なインテリジェンスとして照らし出す知財のホワイトスペースは、未知の疾患に苦しむ患者に新たな治療の希望を届けるための重要な道標であると同時に、企業価値を飛躍的に向上させ、業界全体のオープンイノベーションを強力に推進するための次世代の経済的フロンティアに他なりません。
(この記事はAIを用いて作成しています。)
- DrugPatentWatch, “A strategic guide to white space analysis for pharmaceutical R&D”, https://www.drugpatentwatch.com/blog/a-strategic-guide-to-white-space-analysis-for-pharmaceutical-rd/
- DrugPatentWatch, “AI’s breakthrough applications in pharmaceutical patent analysis and strategy”, https://www.drugpatentwatch.com/blog/ais-breakthrough-applications-in-pharmaceutical-patent-analysis-and-strategy/
- GreyB, “White Space Analysis”, https://greyb.com/services/open-innovation/white-space-analysis/
- Minesoft, “Semantic mapping in patent analysis”, https://minesoft.com/semantic-mapping-in-patent-analysis/
- NCBI, “Large Language Model, Transformer Models…”, https://pmc.ncbi.nlm.nih.gov/articles/PMC10874304/
- Tandfonline, “Natural Language Processing in drug discovery”, https://www.tandfonline.com/doi/full/10.1080/17460441.2025.2490835
- DrugPatentWatch, “How AI and machine learning are forging the next frontier of pharmaceutical IP strategy”, https://www.drugpatentwatch.com/blog/how-ai-and-machine-learning-are-forging-the-next-frontier-of-pharmaceutical-ip-strategy/
- Medable, “Eliminate clinical trial white space with the right AI strategy”, https://www.medable.com/knowledge-center/long-form-eliminate-clinical-trial-white-space-with-the-right-ai-strategy
- Pharmaphorum, “Leveraging AI agents eliminate white space clinical trials”, https://pharmaphorum.com/rd/leveraging-ai-agents-eliminate-white-space-clinical-trials
- McKinsey & Company, “Unlocking peak operational performance in clinical development with artificial intelligence”, https://www.mckinsey.com/industries/life-sciences/our-insights/unlocking-peak-operational-performance-in-clinical-development-with-artificial-intelligence
- 2 Minute Medicine, “Artificial intelligence designed drugs Hit 90% Phase I success rate in trials”, https://www.2minutemedicine.com/ai-designed-drugs-hit-90-phase-i-success-rate-in-trials/
- NCBI, “Adaptive Trial Designs Enhanced by AI”, https://pmc.ncbi.nlm.nih.gov/articles/PMC12627430/
- Insilico Medicine, “Portfolio Strategy: The Medium Novelty Sweet Spot”, https://insilico.com/casestudy
- Insilico Medicine, “LEGION”, https://insilico.com/blog/legion
- DrugPatentWatch, “The new prescription for IP: a strategic guide to patenting AI-derived drugs”, https://www.drugpatentwatch.com/blog/the-new-prescription-for-ip-a-strategic-guide-to-patenting-ai-derived-drugs/